|
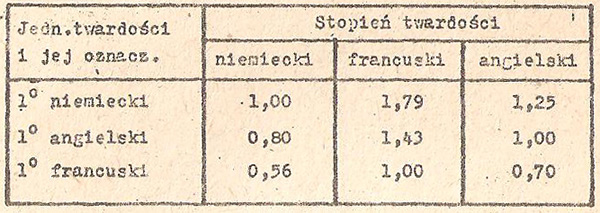
Wprowadzenie do chemii wody Henryk K i l k a Artykuł ten ma stanowić wstęp do cyklu zagadnień wody, jakie będą się ukazywały w naszym dwumiesięczniku. Ażeby jednak problematyka wody omawiana była w sposób zrozumiały, trzeba wyjaśnić sobie pewne podstawowe pojęcia o wodzie i ustalić terminy /słownictwo/, którymi w przyszłości posługiwać się będziemy. Należy zdawać sobie sprawę z tego, że posługiwanie się różnymi określeniami, nastręcza duże kłopoty zarówno dla czytelnika i autora. Redakcja 1. Wstęp Woda występuje powszechnie w przyrodzie i bierze udział we wszystkich procesach biochemicznych, ponadto jest obecna w większości ciał. Dla niezliczonej ilości organizmów jest miejscem życia /egzystencji/. Ogólna ilość wody na globie ziemskim szacowana jest na 2,1018 ton, pokrywa ona około 3/4 powierzchni ziemi. Woda spotykana w przyrodzie i badana pod względem woni, smaku i barwy, wykazuje często różnice. I tak np.: wody morskie czy oceaniczne mają smak słony, a po odparowaniu pozostawiają osad; niektóre wody mineralne burzą się wydzielając z siebie gazy, inne są lekko zabarwione i mają woń gnijących roślin. Wszystkie te różnice biorą początek nie z rozmaitych własności samej wody, lecz z jej zanieczyszczeń, pochodzących z warstw ziemi, przez które ona przepływa. Zanieczyszczeniami tymi mogą być ciała stałe lub gazowe, znacznie rzadziej – ciecze. 2. Rodzaje wód naturalnych Wodę spotykaną w przyrodzie podzielić możemy na kilka rodzajów, w szczególności na : a). W o d a d e s z c z o w a, która jest jedynym źródłem powstawania wód powierzchniowych. Jest to jeden z gatunków najmniej zanieczyszczonej wody naturalnej. Zawiera zazwyczaj rozpuszczone w małych ilościach /kilka miligramów na litr/ gazy powietrza. Woda deszczowa pod postacią śniegu zawiera podobne zanieczyszczenia. b). W o d a p o w i e r z c h n i o w a, zawiera podobne zanieczyszczenia jak woda deszczowa, z której pochodzi, obfituje jednak zwykle w składniki humusowe. c). W o d a ź r ó d l a n a, pochodząca z głębszych warstw ziemi, na skutek naturalnego przefiltrowania nie zawiera prawie wcale bakterii chorobotwórczych, natomiast w znacznych ilościach sole mineralne. Im głębiej woda przenika przez warstwy ziemi, tym bardziej zmniejsza się w niej ilość tlenu /rozpuszczanego/ , a wzrasta zawartość CO2 /dwutlenek węgla/ d). W o d a r z e c z n a, zawiera składniki wód powierzchniowych i źródlanych. Pojawiają się w niej ponadto składniki, które pochodzą ze ścieków. e). W o d a m o r s k a, znajdujemy w niej bardzo znaczne ilości rozpuszczanych soli mineralnych zwłaszcza chlorki sodu /NaCl/, potasu /KCl/ i magnezu /MgCl2/, oraz siarczanu potasu /K2SO4/, wapnia /CaSO4/ i magnezu /MgSO4/. 3. Woda chemicznie czysta; Otrzymanie takiej wody jest bardzo trudne; dochodzi się do niej drogą destylacji i stąd nazwano ją wodą destylowaną. Z wyżej opisanych wód, najbardziej nas interesować będzie woda źródlana, zawierająca w znacznych ilościach sole mineralne. Oddzielną grupę zanieczyszczeń w niej stanowią sole wapniowe i magnezowe, których obecność tworzy tzw. twardość wody. 4. Twardość wody /Tw/ Rozróżniamy następujące rodzaje twardości : a). Twardość ogólna, całkowita /Two/ Suma twardości węglanowej /niesłusznie zwaną dawniej przemijająca / i nie węglanowej stała stanowi twardość ogólną : zwaną również całkowitą. Twardość węglanową, tworzą węglany wapniowe i magnezowe, drugą – pozostałe sole tych metali jak to widać z zestawienia poniżej : Nazwa „twardości przemijającej” pochodzi od właściwości częściowego wytrącania sił z roztworu węglanów wapniowych i magnezowych przy podgrzaniu w następstwie rozkładu chemicznego. Ca/HCO3/2 ————— CaCO3 + CO2 + H2O Sole tworzące twardość stałą przy podgrzewaniu wody nie rozkładają się i nie wytrącają się ; stąd też pochodzi nazwa „twardość stała”. W literaturze niemieckiej twardość w/w podawane są skrótami : G H – oznacza twardość całkowitą Można się również spotkać z innymi symbolami jak np.: dGH względnie dHG, gdzie indeks d oznacza stopień niemiecki /°d/: zaś GH – twardość całkowitą a HG – stopień twardości. Twardość wody jest wyrażona w stopniach twardości określających ilość gramów tlenku wapniowego lub węglanu wapniowego w litrze wody. W poszczególnych krajach używane są różne jednostki twardości. 1° niemiecki twardości /1°n/ = 10 mg CaO/l Obecnie w Polsce rozpowszechnione jest mierzenie twardości wody w stopniach niemieckich z symbolem ° n dawniej stosowano znak ° d. Zależność między poszczególnymi stopniami twardości obrazuje poniższa tabelka. Z tabelki wynika, że 1 ° niemiecki odpowiada 1,79 ° franc, albo 1,25 ° angiel. Na zakończenie zwracam się do wszystkich miłośników hodowli ryb egzotycznych, którzy pragną podzielić się ze swoimi wiadomościami na łamach dwumiesięcznika „Akwarium”, względnie pogłębić swoją wiedzę, ażeby w artykułach nadsyłanych do redakcji, używali terminów i skrótów ogólnie przyjętych w polskiej literaturze fachowej. Poniżej podaję jeszcze raz przyjęte terminy ; – twardość wody – skrót Tw |